morfologie
Při makroskopické úrovni lze při Alzheimerově chorobě pozorovat variabilní stupeň kortikální atrofie (redukce tkáně nebo orgánové hmoty), charakterizované zvětšením parietálních rýh, které jsou výraznější v čelních, časových a parietálních lalocích. Tato atrofie je kompenzována zvětšením komorových dutin sekundárních ke ztrátě parenchymu (obrázek 1). Zejména v pokročilých stádiích nemoci, struktury mediálního spánkového laloku, včetně hipokampu, entorhinalního kortexu a amygdaly, atroficky vážně, vzhledem k jejich zapojení od raných stadií patologie.
Alzheimerova choroba také představuje mikroskopické změny, známé jako extracelulární senilní plaky a intracelulární neurofibrilární klastry, které představují základ histologické diagnózy. S progresí onemocnění pak existuje vážná ztráta neuronů doprovázená gliózou (ohraničená nebo difúzní proliferace, reaktivní v přírodě, neuroglenových buněk, tj. Buněk, které tvoří podpůrné stromum nervové tkáně) ve stejných oblastech kde přítomnost neurofibrilárních plaků a shluků je větší.
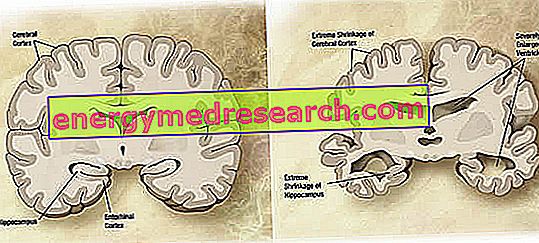
Obrázek 1. Koronální řez mozku: rozdíly mezi normálním mozkem a mozkem postiženým AD (zdroj obrazu wikipedia).
patogeneze
Alzheimerova choroba je charakterizována hlavně dvěma typickými lézemi: extracelulární akumulací senilních plaků sestávajících hlavně z p-amyloidního peptidu (Ap) a intraneuronálních neurofibrilárních klastrů, tvořených hyperfosforylovaným tau proteinem.
- Senilní plaky lze nalézt na úrovni oblastí mozku, jako je hippocampus, amygdala a neocortex.
Ap peptid pochází z proteolytického štěpení prekurzoru amyloidního proteinu (APP) pomocí p-sekretázy. Tento řez vytváří terminální karboxylový fragment 99 zbytků (CTF nebo C99), který je následně štěpen p-sekretázou za vzniku Ap fragmentů, které mají různé délky. Je známo, že nejhojnějším druhem Ap je fragment Ap40. Další známý fragment vytvořený z proteolytického řezu, méně hojný než Ap40, je Ap42, více náchylný k tvorbě amyloidních fibril, které se akumulují jako druhy Ap v mozku jedince s Alzheimerovou chorobou.
- Další složka přítomná v Alzheimerově chorobě je reprezentována neurofibrilárními shluky složenými ze svazků vláken přítomných v cytoplazmě neuronů. Neurofibrilární klastry jsou nerozpustné a zdá se, že jsou rezistentní vůči proteolytickým procesům in vivo, takže zůstávají přítomné v řezech tkáně i po dlouhé době po smrti neuronů. Pozorováním struktury jsou fibrilární shluky tvořeny dvojitými spirálovými vlákny a lineárními filamenty podobného složení. Analýzou kompozice jsou vlákna dvojité šroubovice většinou tvořena hyperfosforylovaným tau proteinem. Tau je axonální protein spojený s mikrotubuly, který usnadňuje jeho sestavení.
Další důležité neuropatologické změny přítomné u Alzheimerovy choroby zahrnují mitochondriální dysfunkci, oxidační poškození neuronů, synaptickou ztrátu a axonální degeneraci.
Neurochemické aspekty
Jak již bylo vysvětleno, peptid Ap pocházející z proteolytického štěpení prekurzoru APP představuje neurotoxickou složku Alzheimerovy choroby . Konkrétně se předpokládalo, že Ap může být důležitý pro normální mozkové funkce, a pokud překoná určité koncentrace, může se stát neurotoxickým. Kromě toho jak agregáty, tak různé izoformy Ap by mohly mít odlišnou biologickou, fyziologickou nebo patologickou úlohu, určování a účast v následných stadiích onemocnění. Bylo pozorováno, že Ap působí jako neuromodulátor, který ovlivňuje uvolňování některých neurotransmiterů v nepřítomnosti zjevných známek neurotoxicity.
Například neuromodulační úloha Ap ve fyziologickém kontextu by mohla mít důležitý význam pro správnou rovnováhu neurotransmiterového systému. Je dobře známo, že tento systém je tvořen neurotransmitery, látkami, které přenášejí informace mezi buňkami, které tvoří nervový systém, neurony, přes synaptický přenos.
U patologických stavů na druhé straně může být AP-zprostředkovaný synaptický přenos spojen se změnou neurotransmise před neurodegenerativními událostmi. V důsledku těchto změn mohou vzniknout časné kognitivní a nekognitivní poruchy, založené na neurotransmiterových systémech a různých oblastech mozku.
Změny systémů neurotransmiterů a mechanismus přenosu signálu v mozku jedinců trpících Alzheimerovou chorobou jsou velmi složité. Jeden ze systémů, který se zdá být změněn, se týká cholinergního signalizačního systému, který zahrnuje neurotransmiter acetylcholin. Bylo prokázáno, že jedinci trpící Alzheimerovou chorobou vykazují sníženou cholinergní transmisi na úrovni kortexu a hipokampu, což jsou důležité oblasti mozku věnované jevům, jako je učení a paměť. Kromě tohoto neurotransmiterového systému byly u Alzheimerovy choroby pozorovány změny noradrenergního, serotonergního a glutamátového a GABA systému.



