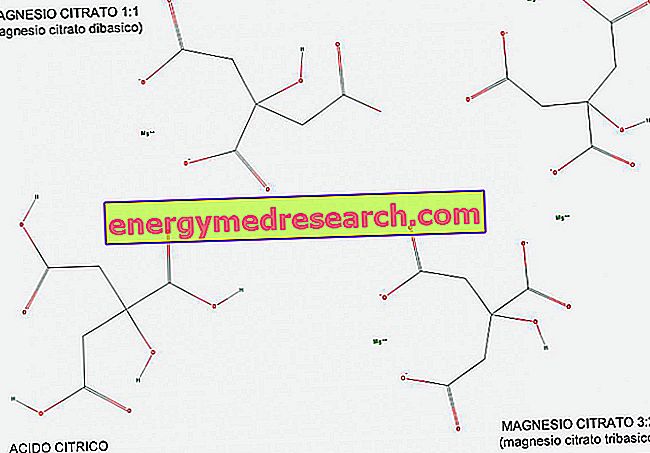
Kyselina tribasová (nebo triprotická) je kyselina, která má tři vodíkové ionty k darování v kyselinové reakci. Pomocí obrázku můžeme vidět, jak je kyselina citrónová příkladem kyseliny tribasové, protože má tři karboxylové skupiny COOH, které mohou snadno přenášet vodík H.
Citrát hořečnatý existuje v poměru 1: 1 (1 molekula hořčíku na molekulu citrátu) a v poměru 3: 2 (3 molekuly hořčíku na 2 molekuly citrátu).
1: 1 citrát hořečnatý se nazývá dibasický, protože se jedná o dvojsytnou sůl kyseliny citrónové; ve skutečnosti má na molekulu 2 univalentní bazické skupiny (COO-), odvozené od 2 karboxylových skupin, které během reakce opustily vodík.
3: 2 hořčík, na druhé straně, je nazýván tribasic protože to má 3 univalentní základní skupiny (COO-) na molekulu, odvozený z 3 karboxylových skupin, které vzdaly se jejich vodíku během reakce.
Citran hořečnatý je jasně bohatší na hořčík (+ 42, 6% hmotnostních) než citronan hořečnatý; navíc je to více alkalizující, protože může přijímat tři vodíkové ionty H + proti dvěma akceptovaným dibasickým iontem. Je však méně rozpustný ve vodě.